
不同物種的端粒序列各有差異,與端粒結合蛋白共同演化、相互適配。發表於《自然通訊》(影響因子14.74)的最新機制研究,以工程酵母菌為模型,將原生端粒序列替換為人類型重複序列,觀察細胞在「序列劇變」後的分子應對。研究發現,替換初期導致基因組不穩定、蛋白質組重塑與嚴重適應度下降;但在持續選擇壓力下,細胞反覆演化出兩類高度收斂的救援突變——端粒結合蛋白基因TBF1擴增,或DNA損傷反應減弱——共同勾勒出端粒重編程後的適應性分子全景,為理解老化與端粒危機提供重要思考框架。

想像一下,把一段「外語指令」悄悄植入細胞核最深處。端粒,原本是染色體末端以「母語」寫就的保護帽,突然換成了完全陌生的「外來腔調」——細胞能活下去嗎?又會如何自救?
端粒序列是染色體末端的重複性DNA,負責防止每次細胞分裂後遺傳訊息流失。然而,端粒序列並非萬物共用一套:酵母菌、果蠅、人類各有其「方言」,且端粒序列與對應的端粒結合蛋白長期共同演化,形成高度適配的分子伙伴關係。這種「共演化」在既有物種間無縫運作,但其底層分子機制卻難以從現存物種的比較中直接推算。
發表於《自然通訊》(Nature Communications,影響因子14.74)的這項研究,正是為了回答一個演化生物學的核心謎題:當端粒序列突然被替換,生命體究竟如何從分子混亂中重建秩序?研究結果所揭示的「適應地圖」,不僅深化了我們對端粒老化機制的認識,也為探索癌症與衰老的分子基礎開啟了新視角。
研究團隊採用釀酒酵母菌(Saccharomyces cerevisiae)作為模式生物,設計多株攜帶人類型端粒重複序列的工程品系,並以保留原生端粒序列的品系為對照組。這是一項機制型實驗室研究,結合基因工程改造與適應性演化(adaptive evolution)雙重設計,系統性追蹤酵母菌在端粒重編程後的分子反應。
研究結果呈現出清晰的兩階段動態。在序列替換的初期,細胞承受了三重打擊:基因組不穩定性顯著上升、全細胞蛋白質組發生大規模重塑,以及整體適應度嚴重下降。這些初期紊亂,反映了原有端粒結合蛋白與新序列之間的深層不匹配——蛋白質尚未「認識」這套新語言,保護機制因此失靈。
然而在持續選擇壓力下,適應性演化實驗篩選出兩類在多個獨立品系中反覆出現(recurrent)的適應性突變。第一類是端粒結合蛋白基因TBF1透過複雜非整倍體(complex aneuploidies)機制擴增;第二類是減弱DNA損傷反應的突變。兩者均在不同演化品系中獨立重複出現,顯示適應路徑具有高度收斂性——細胞面臨相同的端粒危機,傾向走向相同的分子出路。
需如實說明的是,現有摘錄資料未提供具體突變頻率的量化數據或統計顯著性檢驗值(p值),相關精確數據需參閱原始全文。研究的主要限制包括:本實驗僅以酵母菌為模型,與高等真核生物(包括人類)的端粒生物學存在根本差異;實驗室條件下的人工選擇壓力,也無法完整重現自然演化情境;此外,工程化序列替換屬於人為劇烈介入,與物種間長達數百萬年的自然共演化過程不可直接類比。
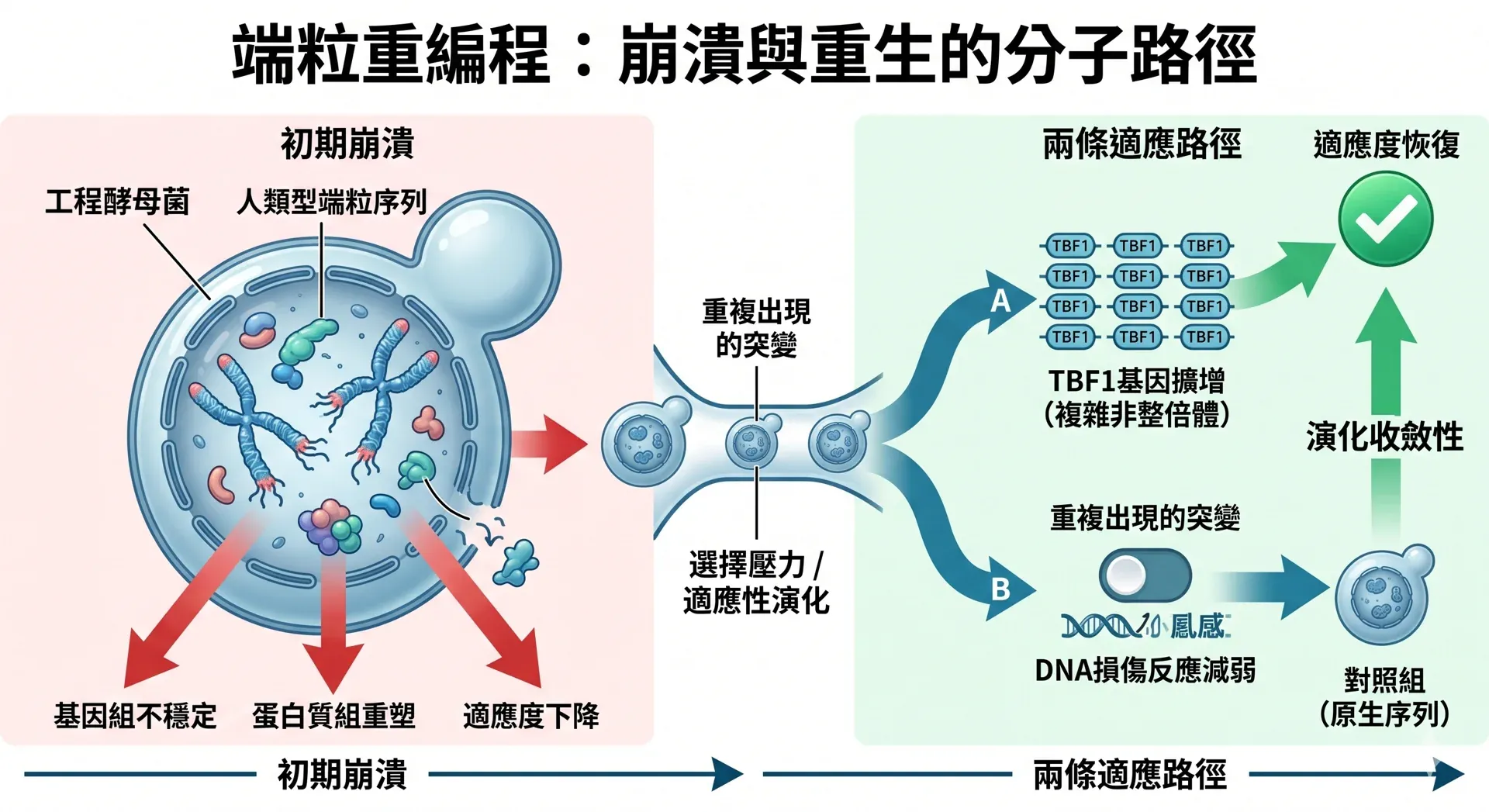
這項研究最引人深思之處,不在於「序列替換後細胞會崩潰」——那幾乎在意料之中——而在於「細胞如何以兩條固定路徑自救」。
TBF1擴增與DNA損傷反應減弱,在多個獨立演化品系中反覆出現,揭示了端粒適應的「最小阻力方向」。這種演化收斂性(evolutionary convergence)告訴我們:面對端粒危機,細胞並非隨機摸索,而是有其固定的應急手冊。這一發現,對於理解老化過程中端粒功能的逐步喪失,或癌細胞如何「黑入」端粒維護機制,都提供了重要的預測性框架。
對於關心自身端粒健康的讀者,這項以酵母菌為材料的基礎研究,仍帶來幾個值得內化的思考方向。
第一,端粒結合蛋白的充足性至關重要。TBF1的擴增是細胞在危機中最快採取的自救策略之一,也提醒我們:人類細胞中,維持shelterin等端粒保護蛋白複合體的正常功能,是染色體穩定的第一道防線。慢性壓力、睡眠剝奪與營養失衡,均已被其他研究指出會影響端粒維護效能。
第二,DNA損傷反應是把雙面刃。短期減弱損傷反應或許能暫時提升細胞適應度,但長期可能累積基因組錯誤,埋下後患。這或許解釋了為何某些抗衰老介入策略,必須在「促進修復」與「避免過度炎症」之間謹慎拿捏。
第三,演化收斂性提供了預測窗口。當不同品系在同樣壓力下選擇相同突變路徑,這類資訊有助於科學家預測:哪些基因或路徑最可能在人類端粒老化過程中率先發生改變,進而提前設計干預策略。
中華端粒協會持續追蹤來自頂尖期刊的最前沿端粒科學研究,將複雜的分子機制轉譯為可信、可讀的健康知識。關注學會,與台灣最專業的端粒科學社群一起,探索長壽與細胞健康的分子密碼。
酵母菌的原生端粒重複序列與人類的(TTAGGG)n不同,兩者各自與對應的端粒結合蛋白共演化,形成高度適配的保護系統。科學家選用酵母菌,是因為它基因操作便利、世代短、易於追蹤演化動態,是研究細胞基礎機制的經典模型。雖然結果不能直接套用於人類,但揭示的分子邏輯可為哺乳類研究提供重要假說與方向。
TBF1是一種端粒結合蛋白基因。當酵母菌的端粒序列被替換為人類型重複序列後,原有端粒蛋白無法有效辨識新序列。細胞透過複雜非整倍體(染色體數目異常)機制大量複製TBF1基因,藉此增加能辨識新序列的蛋白質數量,補足保護缺口。這是一種「量取勝」的應急策略,說明端粒結合蛋白的充足性對維持基因組穩定性具有關鍵地位。
短期而言,在端粒序列替換造成的混亂中,減弱DNA損傷反應可讓細胞暫時停止過度的警報反應,恢復部分適應度。然而長期而言,損傷反應是基因組完整性的守門員,過度抑制可能導致基因突變累積,甚至增加細胞癌化風險。因此,這種「以犧牲精準修復換取短期存活」的策略,在人類健康情境下需要謹慎看待,不宜一概而論地視為正面適應。
這項研究揭示了端粒危機下的「演化收斂路徑」,說明細胞在端粒功能受損時,傾向採用固定的分子解方。對人類醫學而言,此一發現有助於科學家預測老化或疾病過程中端粒相關基因的改變模式,進而設計更精準的干預策略。此外,癌細胞常以非典型機制維持端粒長度,理解端粒適應的分子全景,也有助於識別潛在的抗癌靶點。
想了解更多關於端粒科學的最新研究嗎?中華端粒協會持續追蹤前沿文獻,為您提供科學嚴謹、去除炒作的第一手解讀。