
癌症治療的成效追蹤,長期依賴侵入性切片或高成本影像檢查。一項發表於《ACS Nano》(影響因子13.67)的概念驗證研究,提出以「雙酶驅動奈米感測器」將腫瘤細胞內的端粒酶與APE1活性轉化為可在尿液中偵測的訊號,搭配低成本側流免疫試紙完成目視判讀,無需任何儀器。儘管臨床驗證尚在起步階段,此研究為無創伴隨診斷勾勒出令人期待的技術藍圖,也再次彰顯端粒酶作為腫瘤生物標記物的核心地位。中華端粒協會持續追蹤此領域進展,為讀者提供科學嚴謹、去除炒作的第一手解讀。

每當腫瘤治療進入關鍵節點,患者心中最迫切的問題往往是:「這個療程真的有效嗎?」要回答這個問題,傳統上需要組織切片、電腦斷層掃描,或高度技術依賴的血液生物標記物分析。這些方法不僅耗時費力,對患者而言也是生理與心理的雙重考驗。
端粒酶早已是癌症生物學的核心標誌之一。在超過85%的惡性腫瘤中,端粒酶呈現病理性的異常高表現,而正常體細胞幾乎偵測不到其活性。另一種DNA修復酵素APE1(嘌呤嘧啶核苷酸內切酶1),同樣在多種癌症類型中顯示出過度表現,與腫瘤侵襲性及預後不良密切相關。這兩種酵素的異常活性,不只是腫瘤存在的靜態指紋,更可能是動態追蹤治療反應的即時窗口。
發表於頂級期刊《ACS Nano》(影響因子13.67)的最新研究,提出了一個從根本上翻轉診斷邏輯的解方:透過精心設計的奈米感測器,將腫瘤細胞內部的酵素活性轉化為可在尿液中穩定偵測的訊號,最終以一張低成本的側流免疫試紙(LFA)完成目視判讀。無需儀器,無需專業實驗室——這正是本文要深入解析的技術突破。
本研究屬於機制性概念驗證(proof-of-concept)設計,研究對象為體外(in vitro)癌症相關生物樣本環境,其中APE1與端粒酶呈病理性過度表現。研究目前尚未涵蓋人體臨床試驗或動物模型,屬於技術可行性探索階段,非隨機對照試驗(RCT)或世代研究。
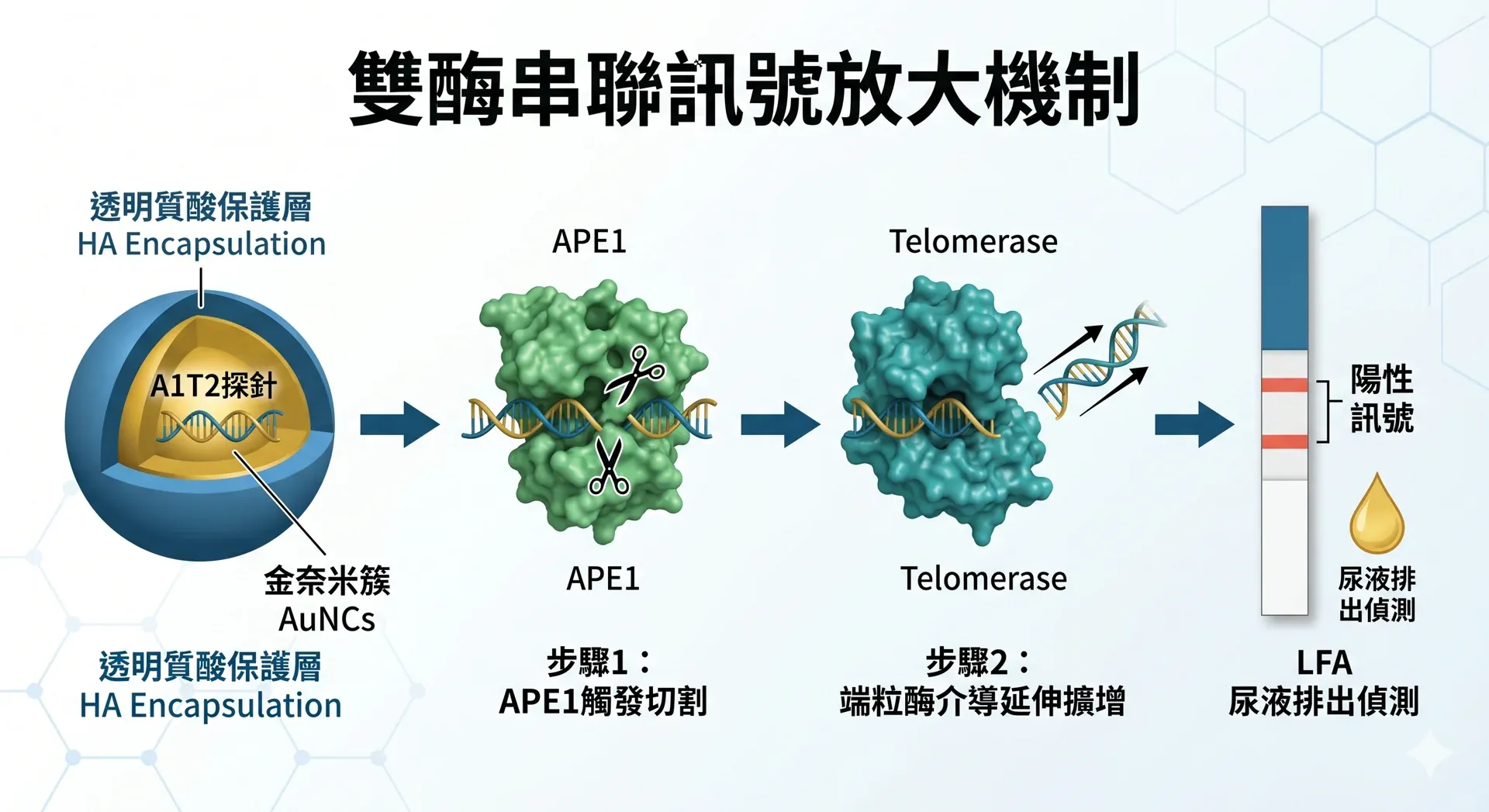
奈米感測器的三層核心設計如下:
第一層,金奈米簇(AuNCs)作為訊號基底。金奈米簇具備固有螢光特性,能夠提供即時監測能力,並顯著強化後續DNA探針的結構穩定性,確保感測器在複雜生物環境中不失效。
第二層,A1T2合成DNA探針作為雙酶識別核心。這條合成DNA序列同時攜帶APE1的識別位點與端粒酶的模板序列,形成「先切割、再延伸」的序列性酵素反應機制。當APE1存在時,A1T2探針在特定位點發生鏈切割;切割後的片段再由端粒酶介導進行延伸擴增,構成雙重訊號放大迴路。
第三層,透明質酸(HA)封裝保護層。整個感測器外覆透明質酸,提供生物相容性保護,維持結構完整性以應對生物環境中的各種干擾。
作用流程可概括為四個步驟:奈米感測器進入腫瘤相關環境後,受APE1活化觸發A1T2探針的鏈切割;端粒酶接著對短片段進行延伸擴增;AuNC標記的短單鏈被排出至尿液;尿液中的短鏈片段透過競爭性LFA策略,在試紙上產生可目視判讀的顯色轉變(chromogenic shift)。研究指出,APE1與端粒酶的協同作用賦予DNA受質「競爭優勢」,使試紙上的顯色訊號獲得增強,進而提升目視解析度。
研究限制方面,須誠實指出以下重要缺口: 本文提供的摘要與前言段落均未揭露任何定量性能指標,包括偵測極限、靈敏度、特異性、訊噪比,亦無p值或信賴區間等統計數據可供評估。這是典型早期機制研究的階段性限制,並非研究的瑕疵,而是提醒讀者:此工具距離臨床應用,尚需完整的體外驗證、動物模型測試、真實尿液基質干擾評估,以及大規模人體臨床試驗的逐步驗證。
從端粒科學的視角解讀這項研究,意義尤為深遠。端粒酶不僅是端粒維護的關鍵酵素,更是細胞不死化(immortalization)的分子開關——而這正是癌症發生的核心機制之一。能在尿液中即時捕捉端粒酶的動態活性,在概念上等同於為腫瘤的「生命力」建立了一扇無創觀測窗。
這項研究代表癌症診斷典範的重要轉移:從被動等待腫瘤自然脫落的生物標記物(常受生理不穩定性與低豐度所困),轉向主動利用腫瘤自身的酵素機器作為訊號轉換媒介。APE1與端粒酶共同「點燃」奈米感測器,將細胞內的分子活動翻譯成可在家中完成的試紙結果——這在設計哲學上是根本性的突破。
然而,誠實的科學傳播要求我們清楚點出現實的距離。從概念驗證到臨床可用工具,往往需要十年以上嚴格的多階段驗證歷程。目前的研究成果仍屬「技術可行性展示」,讀者不宜將其解讀為即將問世的商業產品。
中華端粒協會建議讀者採取以下具體行動:
第一,與主治醫師討論現有的端粒酶相關檢測選項。對於有癌症家族史或正在接受腫瘤治療的朋友,目前已有部分核准的腫瘤標記物檢測可作為追蹤工具,可主動詢問醫師是否適合納入個人化監測計畫。
第二,以「技術成熟度」框架評估新興診斷工具。當媒體報導類似研究時,優先確認該研究是否已完成臨床試驗,並有同儕審查的定量數據支持,避免過早期待尚在實驗階段的技術。
第三,持續關注中華端粒協會的科學追蹤報告。端粒酶與癌症診斷的交叉研究正以前所未有的速度推進,本會持續梳理前沿文獻,為讀者提供有據可查、去除炒作的知識更新。
中華端粒協會相信:讓複雜的分子生物學研究,成為每一位關心健康的知識型讀者都能理解的工具,是我們最重要的使命。追蹤我們,讓科學與您同行。
端粒酶負責維持染色體末端的端粒長度,在正常體細胞中活性極低甚至不可測。然而,超過85%的惡性腫瘤為維持無限增殖能力,會異常高度活化端粒酶。這種「腫瘤特異性高表現」的特性,使端粒酶成為理想的癌症生物標記物候選者。偵測端粒酶活性,理論上可反映腫瘤的存在與動態狀態,而非僅依賴腫瘤脫落的蛋白質碎片。
目前尚不可以。本研究屬於早期機制性概念驗證階段,尚未進入人體臨床試驗,也未揭露偵測靈敏度、特異性等關鍵臨床性能數據。從實驗室概念到醫院可用的診斷工具,通常需要歷經體外驗證、動物安全試驗、第一至三期人體臨床試驗等多個嚴格階段,耗時往往超過十年。建議讀者持續關注後續臨床進展。
APE1(嘌呤嘧啶核苷酸內切酶1)是細胞DNA修復系統中的重要酵素,負責處理氧化損傷造成的無嘌呤/無嘧啶位點。在多種癌症類型中,APE1因腫瘤細胞面臨持續的氧化壓力而過度表現,與腫瘤侵襲性和不良預後相關。在本研究的奈米感測器設計中,APE1作為「第一道觸發訊號」,對DNA探針進行切割,再由端粒酶接力進行擴增延伸,兩者協同放大偵測訊號。
透明質酸是一種廣泛存在於人體結締組織的天然多醣,具有良好的生物相容性。在此奈米感測器中,透明質酸作為封裝保護層,包覆在金奈米簇與DNA探針複合體外側,其作用是維持感測器在複雜生物環境(如細胞質、體液)中的結構完整性,避免提前降解或失活,確保感測器能在正確的時機與位置被腫瘤酵素活化。
側流免疫分析是一種利用毛細現象驅動液體流動、在試紙上呈現目視結果的快速診斷技術。最廣為人知的應用是COVID-19快篩試劑及家用妊娠試紙。本研究中的競爭性LFA策略,將奈米感測器處理後排入尿液的AuNC標記短鏈作為偵測靶標,在試紙上產生顯色訊號,讓腫瘤酵素活性的偵測結果可以目視直接判讀,無需電腦或複雜儀器輔助。
想了解更多關於端粒科學的最新研究嗎?中華端粒協會持續追蹤前沿文獻,為您提供科學嚴謹、去除炒作的第一手解讀。